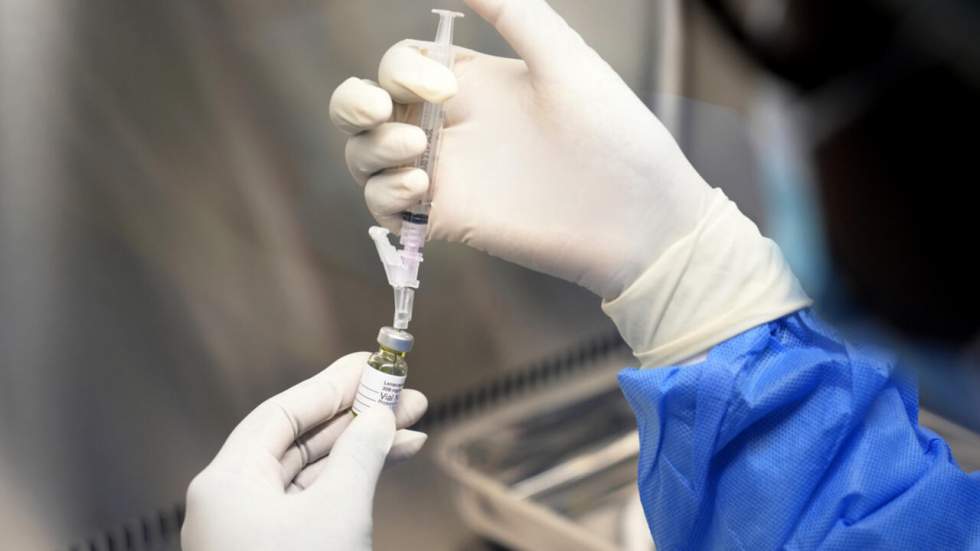
Un pharmacien tient un flacon de lenacapavir, nouveau médicament injectable pour la prévention du VIH, au centre de recherche Masiphumelele de la Desmond Tutu Health Foundation, au Cap, en Afrique du Sud, le 23 juillet 2024. © Nardus Engelbrecht, AP
C'est un espoir majeur dans la prévention du sida, et il pourra bientôt être commercialisé en Europe. Le Yeztugo, baptisé "Yeytuo" sur le vieux continent, a reçu mardi 26 août le feu vert de la Commission européenne.
Ce traitement préventif injectable représente une avancée majeure : deux injections par an suffisent, pour une efficacité proche de 100 %.
Jusqu'ici, la prévention contre le VIH reposait sur un traitement de prophylaxie pré-exposition (PrEP) qui nécessite, elle, la prise d'un comprimé tous les jours à la même heure pendant une certaine période, ou une prise à la demande dans une certaine fenêtre de temps avant un rapport sexuel à risque, puis le lendemain et le surlendemain.
Le mode d'administration simplifié du Yeytuo fait ainsi espérer une meilleure prévention au sein des populations à risque, alors que chaque année, quelque "25 000 nouveaux cas positifs au VIH" sont enregistrés dans l'UE et l'Espace économique européen.
Mais derrière cet espoir immense se profile un obstacle majeur : le coût du traitement qui pourrait freiner son déploiement à grande échelle.
"Ce médicament dépasse les rêves les plus fous"
Le lenacapavir, commercialisé aux États-Unis sous les noms Yeztugo ou Sunlenca a été développé par le laboratoire pharmaceutique américain Gilead Sciences. Issu de la recherche sur la protéine de capside conique du VIH, le lenacapavir prévient presque totalement toute nouvelle infection par le virus.
En décembre 2024, le magazine Science le désignait "Breakthrough of the Year", saluant son efficacité révolutionnaire dans des essais pour l'usage prophylactique (PrEP). Une reconnaissance confirmée en juin dernier avec l'approbation par la Food and Drugs Administration (FDA) du lenacapavir comme premier traitement prophylactique à effet long (six mois) contre le VIH.
"Ce médicament, administré seulement deux fois par an, a montré des résultats remarquables lors d'études cliniques, ce qui signifie qu'il pourrait transformer la prévention du VIH", déclarait en juin Daniel O'Day, PDG de Gilead Sciences. "Les scientifiques de Gilead ont consacré leur vie à mettre fin au virus, et grâce à l'approbation de Yeztugo par la FDA et en collaboration avec nos nombreux partenaires, nous pouvons désormais contribuer à faire de cet objectif une réalité."
À lire La lutte contre le VIH menacée au niveau mondial par les coupes budgétaires de Donald Trump
"Ce médicament est extraordinaire ; c'est ce qui se rapproche le plus d'un vaccin à notre disposition", déclarait un mois auparavant au magazine Science Meghan Ranney, doyenne de la Yale School of Public Health, expliquant avoir débuté sa carrière au plus fort de la pandémie de sida, dans les années 1980-1990. "Ce médicament dépasse les rêves les plus fous que beaucoup d'entre nous auraient pu imaginer".
Dans deux études (PURPOSE 1 et PURPOSE 2), les scientifiques de Gilead ont démontré que ce médicament était 100 % efficace pour protéger les femmes cisgenres contre le VIH. Chez les hommes ayant des rapports sexuels avec des hommes ou des personnes d'autres identités de genre (hommes et femmes transgenre, et personnes non-binaires), le médicament était efficace à 96 %.
Dans le Time, en juin, le Dr David Ho, professeur de microbiologie, d'immunologie et de médecine à l'Université Columbia estime que "son potentiel pour endiguer l'épidémie est considérable".
Un avis que partage l'OMS qui, à l'occasion de la 13e conférence internationale sur la science du VIH, organisé en juillet à Kigali, au Rwanda, a recommandé l'utilisation du lénacapavir injectable, "susceptible de transformer en profondeur la riposte mondiale contre le VIH".
Cependant, l’enthousiasme concernant son approbation par la FDA puis la Commission européenne est tempéré par la question du coût.
Dans une interview accordée en juin au New York Times, Gilead Sciences annonçait un prix catalogue de plus de 28 000 dollars (24 000 euros) par personne et par an aux États-Unis.
Un prix que les laboratoires justifient par les milliards investis en recherche, essais cliniques et procédures réglementaires, l'exclusivité du brevet, mais aussi en jouant sur la "valeur ajoutée" que représente le traitement. Une stratégie critiquée par de nombreux chercheurs et ONG, qui accusent Gilead de bloquer l'accès à une innovation cruciale pour la santé publique.
Un coût trop élevé, y compris pour les pays à "haut revenu"
"Le lénacapavir pourrait être l'outil dont nous avons besoin pour maîtriser les nouvelles infections, mais seulement s'il est proposé à un prix abordable et accessible à tous ceux qui pourraient en bénéficier", plaidait ainsi en juin Winnie Byanyima, directrice exécutive de l'Onusida, programme commun des Nations unies sur le VIH/Sida.
Évoquant des études montrant que le lénacapavir peut être produit à seulement 40 dollars par personne et par an, cette dernière poursuit : "Si ce médicament révolutionnaire reste inabordable, cela ne changera rien [dans la lutte contre le VIH, NDLR]. J'exhorte Gilead à agir comme il se doit. Baisser le prix, augmenter la production et donner au monde une chance de mettre fin au sida."
Après plusieurs semaines d'appels d'experts et d'associations de malades, Gilead – qui bénéficie d'une situation de monopole – a passé en 2024 un accord avec des fabricants pour produire et vendre des génériques anti-VIH à bas coût dans plus de 100 pays en développement et pour fournir de nombreuses doses.
Le Fonds mondial – un partenariat international doté de 5 milliards de dollars par an ayant pour vocation de vaincre le VIH, la tuberculose, ou encore le paludisme – a quant à lui annoncé en juillet avoir signé un contrat avec Gilead pour procurer aux pays à revenus faibles ou intermédiaires le traitement préventif.
Mais ces accords concernent uniquement l'Afrique, et certaines parties de l'Asie et de l'Amérique latine. Les pays à "haut revenu" (Europe, Amérique du Nord, Japon, Australie) ne sont pas inclus. Ainsi, aucun générique n'y est possible tant que le brevet est en vigueur (jusqu'en 2038), sauf via des licences volontaires – accords en vertu desquels les fabricants de médicaments génériques peuvent produire et vendre dans certains pays des médicaments brevetés à des prix plus bas.
À (re)voir L'augmentation des bébés séropositifs au sida en Afrique du Sud inquiète les autorités
En Europe, la commercialisation du Yeytuo dépend donc désormais de discussions pays par pays sur le tarif et le remboursement. Sollicité mardi par l'AFP au sujet de la tarification envisagée en Europe, le laboratoire n'a pas donné suite dans l'immédiat.
Mais le Dr Andrew Hill, chercheur à l'Université de Liverpool et co-auteur d'une analyse montrant que le lénacapavir peut être produit à moindre coût, l'assure : "Même les pays à revenu élevé ne pourront pas se permettre une utilisation à grande échelle du lénacapavir à des prix supérieurs à 20 000 dollars par an".
Selon l'étude qu'il a menée, en cas de production industrielle à grande échelle (de l'ordre de 5 à 10 millions de doses par an), le coût pourrait descendre à 25 dollars (environ 21 euros) par patient, avec une marge bénéficiaire incluse. Soit un écart de près de mille fois entre le coût de revient potentiel et le prix de vente affiché.
Une autre modélisation scientifique publiée via PubMed évoque une fourchette de 41 à 94 dollars par patient et par an, selon le volume produit (1 à 10 millions de doses par an), si des licences volontaires sont en place, et si les fournisseurs de génériques se multiplient.
Alors qu'en 2023, 39,9 millions de personnes dans le monde vivaient avec le VIH [qui infecte plus d’un million de personnes chaque année], le potentiel des versions génériques à bas coût est considérable, à condition d'établir des licences volontaires et une production industrielle à large échelle. Le coût du traitement pourrait ainsi représenter jusqu'à mille fois moins que le prix catalogue.
L'impact réel de ce traitement "révolutionnaire" dépendra donc de son accessibilité économique, bien plus que de son efficacité clinique.